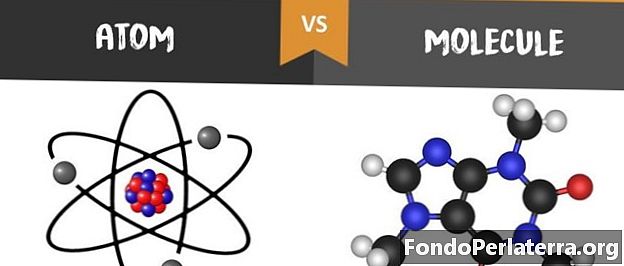
Aatom vs molekul

Sisu
- Sisu: erinevus aatomi ja molekuli vahel
- Võrdlusdiagramm
- Mis on Atom?
- Mis on molekul?
- Peamised erinevused
- Video selgitus
Peamine erinevus aatomi ja molekuli vahel on see, et aatom koosneb neutronitest, prootonitest ja elektronidest, samal ajal kui molekul tähistab aatomite rühma, mis on omavahel seotud kovalentse sideme või ioonse metalli kaudu.
Sisu: erinevus aatomi ja molekuli vahel
- Võrdlusdiagramm
- Mis on Atom?
- Mis on molekul?
- Peamised erinevused
- Video selgitus
Võrdlusdiagramm
| Eristamise alused | Aatom | Molekul |
| Definitsioon | Aatom viitab elementide väikseimale osakesele, mis sisaldab elemendi omadusi | Molekulid tähistavad aatomite rühma või aatomite kombinatsiooni |
| Sõltuvus | Võib või mitte | Jah |
| Materjali omadused | Võib või mitte | Jah |
| Klassifikatsioon | Ei | Kaks: homo- ja heteroaatomi |
| Tugevus | Mateeria peamised ehitusplokid | Inimkehas on rohkem molekule kui tähti universumis |
| Olemasolu | See ei saa iseseisvalt eksisteerida | See võib eksisteerida iseseisvalt |
| Näited | Hapnik, vesinik ja lämmastik | H2, NO jne. |
Mis on Atom?
Aatom tähistab lihtsa aine väikseimat osakeste ühikut, millel on keemilise elemendi omadused. Kõik tüüpi gaasid, tahked ained, vedelikud ja plasma koosnevad ioniseeritud või neutraalsetest aatomitest. Need on tavaliselt väga väikesed ja neid ei saa palja silmaga ega suurendusmikroskoobi kaudu näha. Aatomi suurus võib olla umbes kümme miljardit meetrit. Ma räägin nende piiridest, siis pole neil piire täpselt määratletud.
Füüsika järkjärgulise arenguga on aatomimudelitesse lisatud kvantpõhimõtted, et selgitada aatomi paremat ja ennustatud käitumist. Iga aatom, mis koosneb ühest või enamast tuuma külge seotud elektronist.
Aatomi tuum koosneb ühest või enamast prootonist ja sellel on tavaliselt sarnane arv neutroneid. Aatomi tuuma ümbritsevad ka elektronid, mis on negatiivselt laetud osakesed. Aatom võib olla negatiivselt või positiivselt laetud sõltuvalt enamikust osakestest. Kui need negatiivsed või positiivsed aatomid seovad omavahel molekule, moodustuvad sidemed elektronide kaudu, mis täidavad aatomite välimisi orbiite. Aatomis puudub side, kuna aatomid eksisteerivad iseseisvalt.

Mis on molekul?
Molekul on elektriliselt neutraalse rühma väikseim osake, mis sisaldab selle ühendi või elemendi keemilisi omadusi. Need koosnevad aatomitest, mida hoiavad koos keemilised sidemed. Neid eristatakse ioonidest täielikult elektrilaengu puudumise tõttu.
Enamiku kemikaalide aatomid seovad kiiresti aatomitega molekule. Nende suurus ja keerukus võivad olla erinevad. Need jäävad alati liikuma. Vedelikes ja tahketes ainetes on need tihedalt kokku pakitud. Tahkis olekus saab nende liikumist võrrelda kiire vibratsiooniga. Vedelas olekus liiguvad need üksteise suhtes vabalt omamoodi libisedes. Gaasi olekus on nende tihedus väiksem, võrreldes sama keemilise sideme tahke ja vedelaga, ning liiguvad vedelikuga võrreldes veelgi vabamalt.
Võrreldes aatomiga on molekulil võime iseseisvalt eksisteerida, mis on tingitud aatomis olevast elektronist. Molekulis võib aatom olla stabiilne ainult siis, kui on olemas piisav arv elektrone. Gaaside kineetilise teooria kohaselt kasutatakse molekuli sageli iga gaasilise osakese jaoks, olenemata selle koostisest. Monoatomaatilise molekulaarse struktuuri tõttu peetakse väärisgaasi aatomeid ka molekulideks. ”

Peamised erinevused
- Aatom on elemendi väikseim osake, samal ajal kui molekul on ühendi väikseim osake.
- Aatom võib eksisteerida iseseisvalt või mitte, samas kui molekul eksisteerib alati iseseisvalt.
- Aatomil võivad olla või ei pruugi olla mingi aine omadused, samas kui molekulil on alati aine omadused.
- Molekulid koosnevad aatomitest. Aatom koosneb neutronitest, prootonitest ja elektronidest.
- Aatom võib olla molekul sõltumatu olemasolu tõttu. Aatomid esinevad monoatomilises molekulis selliste stabiilsustegurite tõttu nagu ülladgaasid ja heelium, samas kui molekul ei saa seda aatomit öelda.
- Aatomitel pole enam teisi liike, samas kui molekulidel on kahte tüüpi, mis on homo-aatomi molekulid ja heteroaatomid
- Aatomitel pole üldse sidemeid, samas kui molekulidel on molekulidevahelised jõud ja molekulidevahelised jõud
- Aatomite paigutust saab näha röntgenikiirte abil, samal ajal kui molekulides võimaldab interaktsioon inimesel liikuda, tajuda, paljundada ja palju muud.
- Kolm erinevat tüüpi aatomi on vesinikuaatom, deuteeriumiaatom ja triitium. Kaks tüüpi molekuli on lihtne molekul ja keeruline molekul.
- Aatom ei saa eksisteerida iseseisvalt, samas kui molekul võib eksisteerida iseseisvalt.
- Elemendi aatom ei saa elada vabas olekus, samas kui molekulid võivad elada vabas olekus.
- Aatomi massi ei saa praktiliselt määrata, samal ajal kui üksikute aatomite masside summa moodustab molekuli massi.
- Aatomid võivad ioonide moodustamiseks võita ja kaotada elektrone, samal ajal kui molekulid ei saa ioonide moodustamiseks elektrone võita ega kaota.
- Aatomit on võimatu näha palja silma kaudu ja isegi läbi suurenduse. Molekuli ei saa näha ka palja silmaga, vaid seda saab näha suurendusmikroskoobi kaudu.
- Aatomit ei saa enam jagada, samal ajal kui molekuli saab täiendavalt jagada, et saada üksikuid aatomeid.
- Aatomil on tuuma atraktsioon või side sellega, samal ajal kui molekulil on keemiline atraktsioon või side aatomite vahel.